| 正式な氏名 |
組換えヒトFms関連チロシンキナーゼ3リガンドGMP(rHuFlt-3Ligand) |
| シーケンス |
 |
| アミノ酸配列 |
TQDCSFQHSP ISSDFAVKIR ELSDYLLQDY PVTVASNLQD EELCGGLWRL VLAQRWMERL KTVAGSKMQG LLERVNTEIH FVTKCAFQPP PSCLRFVQTN ISRLLQETSE QLVALKPWIT RQNFSRCLEL QCQPDSSTLP PPWSPRPLEA TAPTA |
| 同義語 |
Flt3L、SLサイトカイン |
| 受入番号 |
P49771 |
| 遺伝子ID |
2323 |
| まとめ |
Flt3-リガンド(FL)は、最近同定された造血サイトカインであり、その活性は膜貫通型糖タンパク質Flt3への結合によって媒介されます。 Flt3は、受容体型チロシンキナーゼ(RTK)のクラスIIIサブファミリーのメンバーとして最初に発見されました。その造血細胞での発現は、高度に濃縮された幹細胞/前駆細胞集団に限定されていることがわかりました。 さらに、クラスIII RTKには、SCF、M-CSF、およびPDGFの受容体が含まれます。 当然のことながら、Flt3-リガンドは構造的にM-CSFおよびSCFにも関連しています。 72つのサイトカインはすべて、I型膜貫通タンパク質と可溶性タンパク質の両方として存在することが示されています。 主要なヒトFLアイソフォームは膜貫通タンパク質であり、タンパク質分解切断を受けて可溶性形態のタンパク質を生成することができます。 ヒトFLの可溶型をコードする選択的スプライシングされたFLmRNAも同定されています。 FLはさまざまなヒトおよびマウス組織で広く発現しています。 アミノ酸配列レベルでは、ヒトとマウスのFLは約XNUMX%同一であり、XNUMXつのタンパク質は異種間活性を示します。 FLは、多種多様な造血サイトカインと相乗作用して、初期の造血前駆細胞の成長と分化を刺激することが示されています。 |
| ソース |
Escherichiacoli。 |
| 分子量 |
約17.6kDa、155個のアミノ酸を含む単一の非グリコシル化ポリペプチド鎖。 |
| 生物活性 |
標準と比較した場合、完全に生物学的に活性です。 ヒトAML50細胞を使用した細胞増殖アッセイによって決定されたED5は、1.0 ng / ml未満であり、> 1.0×106IU / mgの比放射能に対応します。 |
| 外観 |
滅菌濾過された白色の凍結乾燥(凍結乾燥)粉末。 |
| 製剤 |
PBS、pH0.2中の7.0um濾過濃縮溶液から凍結乾燥した。 |
| エンドトキシン |
LAL法で測定した場合、0.01 EU / ug未満のrHuFlt3-リガンドGMP。 |
| 再構成 |
内容物を底に持ってくるために、このバイアルを開く前に簡単に遠心分離することをお勧めします。 0.1%BSAを含む滅菌蒸留水または水性緩衝液で0.1〜1.0 mg / mLの濃度に再構成します。 ストック溶液は、作業アリコートに配分し、-20°C以下で保存する必要があります。 適切な緩衝液でさらに希釈する必要があります。 |
| 安定性と保管 |
手動の霜取り冷凍庫を使用し、凍結融解サイクルを繰り返さないようにします。供給された状態で-12°C以下で保管する場合は最低20か月。 賞味期限については、ロット固有のCOAを参照してください。1か月、再構成後の滅菌条件下で2〜8°C。3か月、再構成後の滅菌条件下で-20〜-70°C。 |
| 参考文献 |
1. Hacein-Bey S、Basile GD、Lemerle J、他。 1998. Blood、92: 4090-7.2。 ピーターズ M、ソレム F、ゴールドシュミット J 他2001. Exp Hematol、29: 146-55.3。 Beq S、Fontanet A、Theze J、他。 2004. エイズ、18: 2089-91.4。 マハデヴァン D、チョイ J、クック L、他2009. ハム ゲノミクス プロテオミクス、2009: 453634。 |
| SDS-PAGE |
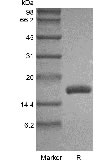 |
| 安全データシート(SDS)ダウンロード |
クリックしてダウンロードする |
| テクニカルデータシート(TDS)のダウンロード |
クリックしてダウンロードする |



